2.2. Mool, mass ja molaarmass
Mool on küll keemikute seas väga laialt kasutatav ühik, aga ühtegi mõõteriista ei saa kasutada otseselt moolide mõõtmiseks. Samuti ei saa osta tavapäraselt lahtiseid komme moolides, vaid ikka grammides. Selleks, et minna ainehulgalt üle massile, kasutatakse molaarmassi. Mis on mooli ja massi seos ning kuidas leida molaarmassi ning molaarmassi kaudu aine massi, saad vaadata järgmisest videost.
Allikas: https://youtu.be/g1s_JY9rcJs
Molaarmass on ühe mooli aineosakeste mass.
Molaarmassi tähiseks on M ning keemias kõige kasutatavamaks molaarmassi ühikuks g/mol. Selleks, et leida konkreetse ühendi molaarmassi, tuleb liita aine koostises olevate elementide ümardatud aatommassid, kusjuures tuleb arvestada ka aatomite arve keemilises valemis.
Näide 1. Arvuta vee molaarmass.
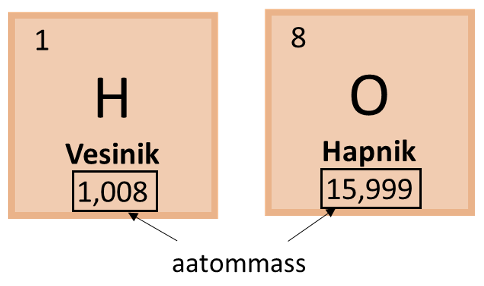 Vee keemiline valem on H2O. Molaarmassi leidmiseks kasutame perioodilisustabelis toodud aatommasse, kuid ümardame need täisarvuks. Vesiniku aatommass on 1.008 ehk ümardatuna täisarvuks 1 ning hapniku aatommass on 15.999 ehk ümardatuna täisarvuks 16. Kuna vee molekulis on 2 vesiniku aatomit, tuleb seda ka arvutuses arvestada ning vee molaarmassi leidmiseks on arvutuskäik järgmine:
Vee keemiline valem on H2O. Molaarmassi leidmiseks kasutame perioodilisustabelis toodud aatommasse, kuid ümardame need täisarvuks. Vesiniku aatommass on 1.008 ehk ümardatuna täisarvuks 1 ning hapniku aatommass on 15.999 ehk ümardatuna täisarvuks 16. Kuna vee molekulis on 2 vesiniku aatomit, tuleb seda ka arvutuses arvestada ning vee molaarmassi leidmiseks on arvutuskäik järgmine:
M(H2O) = 2 $\times $1 + 16 = 18 g/mol
Allpool on toodud mõne ühendi molaarmassid koos arvutuskäiguga. Kontrolli, kas saad samad tulemused.
M(K) = 39 g/mol
M(Al2O3) = 2 $\times $ 27 + 3 $\times $16 = 102 g/mol
M(H2SO3) = 2 $\times $ 1 + 32 + 3 $\times $ 16 = 82 g/mol
M(NaCl) = 23 + 35,5 = 58,5 g/mol
Nagu viimasest näitest selgub, on aatommasside ümardamisel erandeid. Jäta meelde, et kloori aatommassi väärtus on 35,5 ning vase oma 63,5 g/mol.
Vali õige molaarmass.Ülesanne 1
1.1 Liitiumhüdroksiid: 24 g/mol
Lahendus: M(LiOH) = 7 + 16 + 1 = 24 (g/mol)
1.2 Dilämmastikpentaoksiid: 108 g/mol
Lahendus: M(N2O5) = 2×14 + 5 × 16 = 108 (g/mol)
1.3 Naatriumsulfaat: 142 g/mol
Lahendus: M(Na2SO4) = 2×23 + 32 + 4 × 16 = 142 (g/mol)
1.4 Alumiinium(III)sulfaat: 342 g/mol
Lahendus: M[Al2(SO4)3] = 2×27 + 3(32 + 4 × 16) = 342 (g/mol)
1.5 Raud(III)karbonaat: 292 g/mol
Lahendus: M[Fe2(CO3)3] = 2×56 + 3(12 + 3 × 16) = 292 (g/mol)
Ülesande 1 lahendused
Molaarmassi seos ainehulgaga:
$n=\frac{m}{M}$
n - ainehulk (ühik mol)
m - aine mass (ühik g)
M - molaarmass (ühik g/mol)
Molaarmassi kasutades on võimalik arvutada aine hulka või massi. Ainehulk on avaldatav kui $n=\frac{m}{M}$,
kus n tähistab ainehulka (ühik mool, lühend mol), m aine massi (ühik gramm) ning M on molaarmass (ühik g/mol).
Arvutusülesannete lahendamise käiguga oled ilmselt juba tuttav, kuid kordame selle üle.
Arvutusülesannete lihtsamaks lahendamiseks võid eeskujuks võtta järgnevad sammud:
- Loe ülesande tekst mõttega läbi.
- Jooni tekstis alla kõik arvud.
- Omista arvule kindel füüsikaline suurus. Seda on lihtne teha näiteks ühiku alusel.
- Kirjuta välja andmed ning otsitav suurus.
- Kirjuta välja valemid ning kui vaja, avalda valemist otsitav suurus.
- Asenda valemitesse arvud ning arvuta.
Ole valmis, et mõnikord tuleb ühikuid teisendada.
Teeme koos läbi 2 ülesannet.
Näidisülesanne 1. Ainehulga arvutamine
| 1. Loe ülesande tekst mõttega läbi. | Mitu mooli on 9,3 grammis naatriumoksiidis? |
| 2. Jooni alla kõik arvud, mis on tekstis. | Mitu mooli on 9,3 grammis naatriumoksiidis? |
|
3. Omista arvule kindel füüsikaline suurus. |
9,3 grammi näitab aine massi. |
| 4. Kirjuta välja andmed. |
m = 9,3 g Samuti on hetkel teada, et aineks on naatriumoksiid, mille valem on Na2O. Igale ainele, mille valemit sa tead, saab leida molaarmassi. M(Na2O) = 2 $\times $ 23 + 16 = 62 g/mol Otsitav suurus on hetkel moolide arv, järelikult n = ? |
| 5. Kirjuta välja valemid. |
$n=\frac{m}{M}$ Kuna antud juhul on vajalik ainehulk, siis valemist mõnda teist suurust avaldama ei pea. |
| 6. Asenda arvud ja arvuta. | $n=\frac{m}{M}=\frac{9,3\ g}{62\ g/mol}=0,15\ mol$ |
Ülesanne 2
Arvuta ainehulk.
Ülesande 2 lahendused
2.1 Mitu mooli on 3,12 grammi alumiiniumhüdroksiidi? 0,04 mol
Lahendus: 3,12 grammi näitab alumiiniumhüdroksiidi massi m. Alumiiniumhüdroksiidi valem on Al(OH)3, leiame sellele molaarmassi.
M[Al(OH)3] = 27 + 3(16 + 1) = 78 g/mol
Otsitav suurus on moolide arv n.
\(x = {m \over M} = {3.12g\over78 g/mol} = 0.04mol\)
2.2. Mitu mooli on 0,5 kg vääveltrioksiidi? 6,25 mol
Lahendus: 0,5 kg näitab vääveltrioksiidi massi m. Teisendame selle grammideks.
0,5 kg = 500 g
Vääveltrioksiidi valem on SO3, leiame sellele molaarmassi.
M(SO3) = 32 + 3 × 16 = 80 g/mol
Otsitav suurus on moolide arv n.
\(x = {m \over M} = {500g\over80 g/mol} = 6.25mol\)
2.3. Mitu mooli on 800 grammi raud(III)hüdroksiidi? 7,48 mol
Lahendus: 800 g näitab raud(III)hüdroksiidi massi m.
Raud(III)hüdroksiidi valem on Fe(OH)3, leiame sellele molaarmassi.
M[Fe(OH)3] = 56 + 3(16 + 1) = 107 g/mol
Otsitav suurus on moolide arv n.
\(x = {m \over M} = {800g\over 107 g/mol} = 7.48mol\)
2.4. Mitu mooli on 450 g vett? 25 mol
Lahendus: 450 g näitab vee massi m.
Vee molekulvalem on H2O, leiame sellele molaarmassi.
M(H2O) = 2×1 + 16 = 18 g/mol
Otsitav suurus on moolide arv n.
\(x = {m \over M} = {450g\over18 g/mol} = 25mol\)
Näidisülesanne 2. Aine massi arvutamine
| 1. Loe ülesande tekst mõttega läbi. | Arvuta 3 mol kaaliumnitraadi mass. |
| 2. Jooni alla kõik arvud, mis on tekstis. | Arvuta 3 mol kaaliumnitraadi mass. |
| 3. Omista arvule kindel füüsikaline suurus. | 3 mol näitab ainehulka. |
| 4. Kirjuta välja andmed. |
n = 3 mol Samuti on hetkel teada, et aineks on kaaliumnitraat, mille valem on KNO3, mille molaarmass on: M(KNO3) = 39 + 14 + 3 $\times $ 16 = 101 g/mol Otsitav suurus on hetkel mass, järelikult m = ? |
| 5. Kirjuta välja valemid. |
$n=\frac{m}{M}$ Kuna antud juhul on vajalik mass, siis mass avaldub: m = n $\times $ M |
| 6. Asenda arvud ja arvuta. |
m = 3 mol $\times $ 101 g/mol = 303 g Ka ühikutega saad sama tehte teha: mol × g/mol, milles moolid taanduvad maha ning alles jääb massi ühik g. |
Ülesanne 3
Ülesande 3 lahendused
3.1. Kui suur mass on 0,15 mol naatriumhüdroksiidil? 6 g
Lahendus: 0,15 mol näitab ainehulka (moolide arvu) n. Naatriumhüdroksiidi valem on NaOH, sellele saame arvutada molaarmassi.
M(NaOH) = 22 + 16 + 1 = 40 g/mol
Otsitav suurus on mass m.
m = n × M = 0,15 mol × 40 g/mol = 6 g
3.2. Kui suur mass on 31 mmol lämmastikhappel? 1,95 g
Lahendus: 31 mmol näitab ainehulka (moolide arvu) n. Teisendame selle moolideks.
31 mmol = 0,031 mol
Lämmastikhappe valem on HNO3, sellele saame arvutada molaarmassi.
M(HNO3) = 1 + 14 + 3×16 = 63 g/mol
Otsitav suurus on mass m.
m = n × M = 0,031 mol × 63 g/mol = 1,95 g
3.3. Kui suur mass on 6,02×1023 vee molekulil? 18 g
Lahendus: 6,02×1023 näitab vee molekulide arvu N. Kuna alati on teada Avogadro arv NA = 6,02×1023 aatomit/mol, saame leida vee moolide arvu.
\(n={N \over N_A} = {{6.02 * 10^{23} aatomit} \over 6.02 * 10^{23}aatomit/mol} = 1mol\)
Aine massi leidmiseks peame arvutama selle molaarmassi. Vee molekulvalem on H2O, leiame sellele molaarmassi.
M(H2O) = 2×1 + 16 = 18 g/mol
Leiame nüüd otsitava suuruse, massi m:
m = n × M=1 mol × 18 g/mol = 18 g
3.4. Vasta küsimustele.
Lahendus: Arvuta aine molaarmass, kui on teada, et 270 grammis aines oli aine hulk 15 mol. Vastus: 18 g/mol
Teada on aine mass m = 270 g ja aine hulk n = 15 mol. Nende andmetega saame leida otsitava suuruse, molaarmassi M.
\(M ={m \over n}= {270g \over 15 mol} = 18 g/mol\)

