
5.5. Metallide korrosioon
Korrosiooniga oled Sa kindlasti oma elus kokku puutunud: roostes naelad või rattakett, rohekasmusta paatinakihiga kaetud vaskne kirikutorn, hõbedast ehete tumenemine jne. Ülevaate korrosioonist annab allolev video.
Allikas: https://youtu.be/EwiL-4H361U
on protsess, mille käigus toimub metalli hävimine ümbritseva keskkonna toimel. Korrosiooni korral toimub , mille käigus oksüdeeruvad ehk loovutavad elektrone mõnele keskkonnas leiduvale oksüdeerijale (enamasti on selleks õhus leiduv hapnik) ja nii tekib metallist kui lihtainest metalliühend. Tekkival metalliühendil on madalam energia kui puhtal metallil ja seetõttu on ta ka palju püsivam. Kuna korrosiooni korral läheb metall püsivamasse ehk madalama energiaga olekusse (reeglina tekib temast metalli oksiid), siis saamegi järeldada, et korrosioon toimub vastavates keskkonnatingimustes iseeneslikult, selle toimumiseks pole tarvis lisaenergiat.
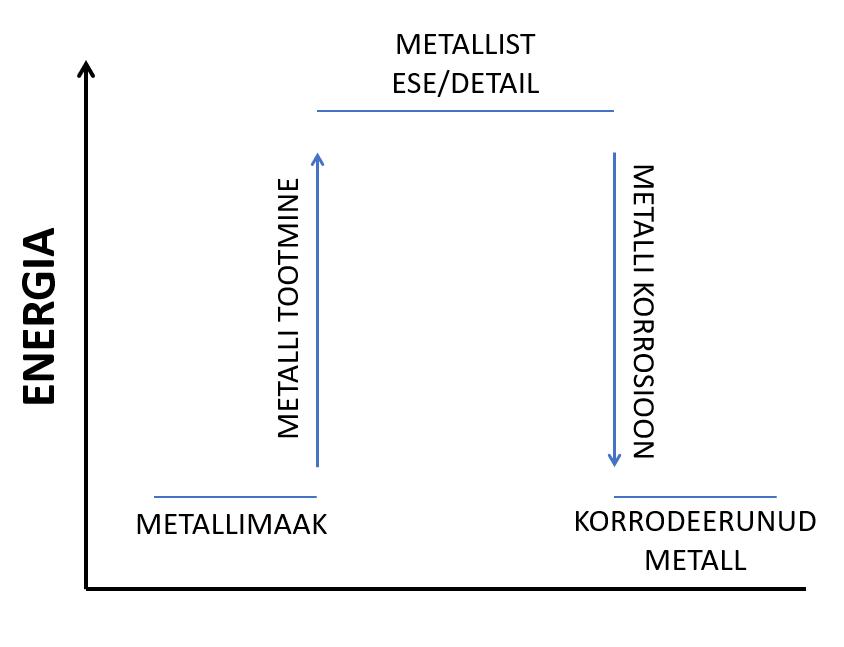
Metallide korrodeerumine
Kuna metallide aktiivsus on küllaltki erinev, kulgeb ka eri metallide korrodeerumine väga erinevalt. Näiteks alumiiniumi, tsingi või nikli pinnale moodustub hapnikuga reageerimise tulemusel tihe ja õhuke oksiidikiht, mis kaitseb metalli edasise oksüdeerumise eest, kuna takistab niiskuse ja hapniku jõudmist metalli pinnani. Seevastu raua pinnale moodustub hapnikuga reageerimisel pudenev rauarooste kiht, mis ei kaitse metalli edasise keskkonnamõju eest, ning seetõttu võivad rauast detailid ümbritseva keskkonna toimel täielikult hävida.
Raua roostetamine
Raua korrosiooni tuntakse igapäevaelus kui raua roostetamist. Raua roostetamine on küllaltki keeruline protsess, kuid lihtsustatult võime seda vaadelda kui raua reaktsiooni hapnikuga, mille tulemusel moodustub punakaspruuni värvusega raud(III)oksiid:
4Fe + 3O2 → 2Fe2O3
Kuna väga paljud inimese jaoks olulised detailid ja esemed on valmistatud rauast või tema sulamitest, on oluline mõista, millised tegurid soodustavad raua roostetamist ja kuidas kaitsta rauast detaile korrosiooni eest.
Raua korrosiooni soodustavad
- niiskus;
- happeline keskkond;
- lahuses esinevad erinevad (sageli kloriidid);
- kõrgem temperatuur;
- kontakt vähemaktiivse metalliga.
Järelikult kui tahame kaitsta rauasulamitest valmistatud esemeid korrosiooni eest, peame tagama, et kuidagi oleks kõrvaldatud korrosiooni soodustavad tegurid ehk peaksime püüdma vähendada kaitstava metalli kontakti väliskeskkonnaga. Seda saab teha näiteks metalli pinna katmisel kas värvi või lakiga, aga ka mõne püsivama metalli kihi või plastikuga. Näiteks jalgratta raam kaetakse värviga, aiamööbli korral kasutatakse plastikust katteid või autode veljed kaetakse kroomiga. Veel kasutatakse korrosiooni tõrjumiseks erisulamite valmistamist. Näiteks selleks, et takistada raua roostetamist, on võimalik valmistada raua ja süsiniku , milles kasutatakse lisandina kroomi. Saadud sulamit nimetatakse roostevabaks teraseks ja see on vastupidav nii niiskuse kui ka õhuhapniku toimele, sest kroomi aatomite oksüdeerumise tulemusel moodustub tugev ja kaitsev oksiidikiht. Korrosiooni takistamiseks kasutatakse ka ohverdusmetalli ehk see metall, mida soovitakse kaitsta väliskeskkonna eest, viiakse kontakti aktiivsema metalliga, mis siis ise oksüdeerub ehk käitub korrosiooni ohvrina. Sellist meetodit kasutatakse näiteks laevade puhul, kus terasest laevakerega ühendatakse näiteks tsingist valmistatud plaadikesed. Kuna tsink on rauaga võrreldes aktiivsem metall, korrodeerub tema enne ja kaitseb nii terasest laevakeret roostetamise eest. Seejuures peab olema tähelepanelik ja asendama tsinkplaadid enne, kui need täielikult oksüdeeruvad.


