
2.3. Keemilised sidemed
Keemiliste sidemete abil moodustuvad aineosakestest erinevad ained. Millised võimalused on keemiliste sidemete tekkeks, tutvustab Sulle järgnev video.
Allikas: https://youtu.be/59Zr7-zeJ8I
on vastastikmõju, mis ühendab aatomid või ioonid molekuliks või kristalliks. Keemilise sideme moodustumisega püüavad osakesed saavutada täielikult täidetud (8 elektroni) välist elektronkihti, sest selline olek on püsivaim. Nendel elementidel, mille elektronkattes on ainult üks elektronkiht, on täielikult täidetud elektronkihil 2 elektroni. Keemilise sideme liigid on , ja . See, milline side tekib, sõltub sellest, millised keemilised elemendid omavahel sideme moodustavad.
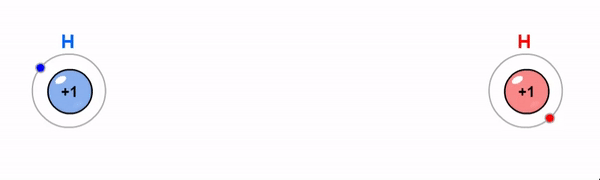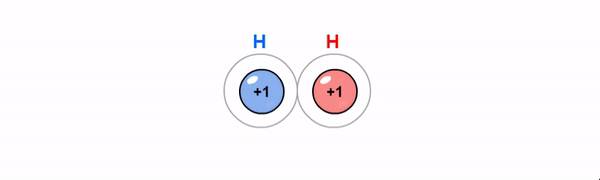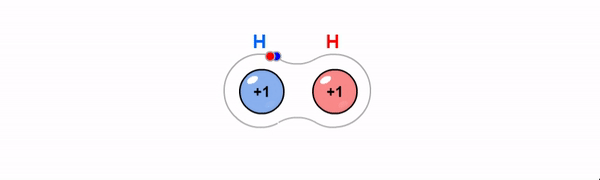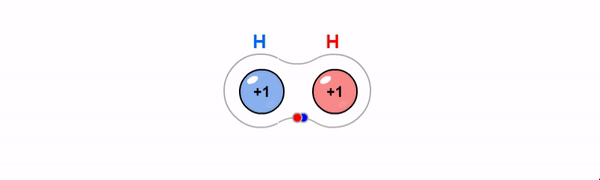
Kovalentne side on ühiste elektronpaaride abil moodustunud keemiline side. Kovalentne side tekib enamasti mittemetalliliste elementide aatomite vahel, kui aatomid moodustavad väliskihi üksikute elektronide abil ühise(d) elektronpaari(d). Maksimaalselt võib moodustuda kahe aatomi vahel kolmekordne side.
Iooniline side on vastasmärgiliste laengutega ioonide tõmbumine. Iooniline side tekib, kui metalli aatomid loovutavad oma elektronkatte väliskihist elektrone mittemetalli aatomite elektonkatte väliskihti.

Metalliline side esineb metallide lihtainetes. Metalliside moodustub metalli kristallvõres paiknevate positiivsete ioonide ja nende ioonide vahel liikuvate ühiste vabade elektronide omavahelisel tõmbumisel.

Ainete omadused sõltuvad nende ehitusest. Seejuures on väga oluline, kas aine koosneb molekulidest või mitte. Sellest lähtuvalt saabki ained liigitada molekulaarseteks ja mittemolekulaarseteks.


