3.5. Soolad
Soolad on igapäevaelus väga laialdaselt kasutuses. Näiteks toitu saad maitsetada soolaga, siin mõeldakse peamiselt naatriumkloriidi ehk NaCl. Kooki saad kergitada vesiniksoola ehk naatriumvesinikkarbonaadiga ehk NaHCO3-ga. Naatriumkloriidi ja kaaliumkloriidi (KCl) sisaldub mineraalvees Värska Originaal.
Soolad on ained, mis koosnevad metalli katioonist ja happejääkioonist ehk happeanioonist. Kuidas soolasid nimetada ja kuidas soolad tekivad, saada vaadata järgmisest videost.
Allikas: https://youtu.be/TQ-110H2mL8
Nimetamine
Soolade nimetamise üldkuju:
katiooni nimi + (o.a) + happejääkiooni nimi
Soolade nimetamisel tee kindlaks, millise metalli katioonist ja millise happe anioonist sool koosneb.
Soolade nimetamise üldkuju: katiooni nimi + (o.a) + happejääkiooni nimi
Happejääkioonide nimed on toodud hapete teema tabelis.
Soolade nimetamisel vaata eelnevalt, kas metalliiooni oksüdatsiooniaste on püsiv või muutuv. Sellest tulenevalt on kaks nimetamise reeglit.
1. Kui soola koostises oleval metallilisel elemendil on püsiv oksüdatsiooniaste, antakse nimetus järgmiselt: metalli nimi + happejääkiooni nimi,
nt NaCl - naatriumkloriid, AlBr3 - alumiiniumbromiid.
2. Kui soola koostises oleval metallilisel elemendil on muutuv oksüdatsiooniaste, antakse nimetus nii: metalli nimi + (o.a) + happejääkiooni nimi,
nt CuCO3 - vask(II)karbonaat, Fe2(SO4)3 - raud(III)sulfaat.
Valemite koostamine
Soola valemi koostamist vaatame kahe näite põhjal.
1. näide. Kirjuta kaltsiumkloriidi valem
- Kirjuta kõigepealt üksteise kõrvale metalli katioon ning seejärel happejääkioon: Ca2+ Cl-.
- Võrdsusta positiivsed ja negatiivsed laengud, et ühend oleks tervikuna neutraalne. Antud näites tuleb anioone võtta 2 tükki.
- Eelnevat arvesse võttes on kaltsiumkloriidi valem CaCl2.
2. näide. Kirjuta raud(III)sulfaadi valem.
- Kirjuta kõigepealt üksteise kõrvale metalli katioon ning seejärel happejääkioon: Fe3+ SO42-.
-
Võrdsusta positiivsed ja negatiivsed laengud, et ühend oleks tervikuna neutraalne. Antud näites tuleb katioone võtta 2 ja anioone võtta 3 tükki.
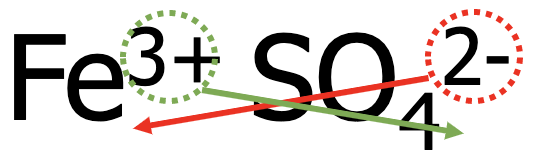
- Eelnevat arvesse võttes on raud(III)sulfaadi valem: Fe2(SO4)3.
Ülesanne 2
Liigitamine
Lihtsoolad koosnevad metalliioonist ja „tavalisest“ happejääkioonist (vt hapete teema tabelit).
Vesiniksoolad koosnevad metalliioonist ja happejääkioonist, mis sisaldab ka vesinikku. Vesinikku sisaldavaid happejääkioone annavad lahusesse mitmeprootonilised happed. Tuntuim vesiniksool on naatriumvesinikkarbonaat (NaHCO3) ehk söögisooda. Vesiniksoolad tekivad aluse ja happe vahelisel reaktsioonil, kui alust ei ole piisavalt happe täielikuks neutraliseerimiseks. Näiteks süsihappe ja kaaliumhüdroksiidi vahelise reaktsiooni tulemusena võib moodustuda nii kaaliumkarbonaat kui ka kaaliumvesinikkarbonaat.
H2CO3 + KOH → KHCO3 + H2O
kaalimvesinikkarbonaat - vesiniksool
H2CO3 + 2KOH → K2CO3 + 2H2O
kaaliumkarbonaat - lihtsool
Nagu näha, kulub ühe osa kaaliumkarbonaadi tekkimiseks 2 osa kaaliumhüdroksiidi, kuid kaaliumvesinikkarbonaadi tekkimiseks kulub vaid üks osa kaaliumhüdroksiidi.
Happed, mis tekitavad vesiniksoolasid ning hapetele vastavad happejääkioonid
|
Hape |
-1 H+ |
-2 H+ |
-3 H+ |
|
H2CO3 |
HCO3- vesinikkarbonaatioon |
CO32- karbonaatioon |
- |
|
H3PO4 |
H2PO4- divesinikfostaatioon |
HPO42- vesinikfostaatioon |
PO43- fosfaatioon |
|
H2SO3 |
HSO3- vesiniksulfitioon |
SO32- sulfitioon |
- |
Neutralisatsioonireaktsioon
Sa oled tuttav juba aluste ja hapete aineklassiga. Mis aga juhtub siis, kui aluse ja happe lahus kokku valada?
Allikas: https://youtu.be/LTnw48BpkwM
Happe ja aluse vaheline reaktsioon on neutralisatsioonireaktsioon. Sa tead juba, et happed on ained, mis annavad vesilahusesse vesinikioone ning alused annavad lahusesse hüdroksiidioone. Siinkohal tähendabki neutraliseerimine olukorda, kus happele on lisatud nii palju alust, et lahuses olevate vesinikioonide happelist mõju vähendatakse hüdroksiidioonidega ning lahus muutub neutraalseks (süsteem toimib ka vastupidi – alusele hapet lisades).
Aluse ja happe vaheline reaktsioon toimub alati, olenemata alusest või happest, mida kasutatakse.
Neutralisatsioonireaktsioon on vahetusreaktsioon, mis tähendab seda, et aluse ja happe samalaengulised ioonid vahetavad kohad. Võttes näiteks liitiumhüdroksiidi ja väävelhappe vahelise reaktsiooni, vahetame positiivsete ioonide asukohad.
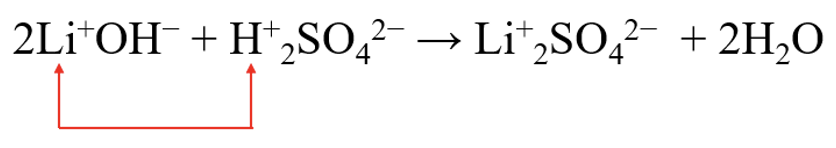
Seega tekivad meile saadustena liitiumsulfaat ja vesi.
2LiOH + H2SO4 → Li2SO4 + 2H2O
Samamoodi toimime kaltsiumhüdroksiidi ja vesinikkloriidhappe vahelise reaktsioonivõrrandi kirjutamisel ehk vahetame kaltsiumiooni ja vesinikiooni asukohad ning selle tulemusel tekivad kaltsiumkloriid ja vesi.
Ca(OH)2 + 2HCl → CaCl2 + H2O
Soolade saamine
Keemilisi reaktsioone, mille käigus soolad moodustuvad, oleme juba oksiidide, hapete ja aluste osas käsitlenud, aga olgu need siin kokkuvõtlikult uuesti kirjas.
1. HAPE + ALUS → SOOL + H2O
HCl + NaOH → NaCl + H2O
See reaktsioon toimub alati.
2. HAPE + METALL → SOOL + H2↑
3H2SO4 + 2Al → Al2(SO4)3 + 3H2↑
See reaktsioon ei toimu alati. Lahjendatud hapetega reageerivad vaid need metallid, mis on vesinikust aktiivsemad ehk asuvad metallide elektrokeemilise aktiivsuse reas vesinikust eespool ehk vesinikust vasakul pool (vt hapete teemat).
3. HAPE + ALUSELINE OKSIID → SOOL + H2O
2HNO3 + CaO → Ca(NO3)2 + H2O
See reaktsioon toimub alati.
4. ALUS + HAPPELINE OKSIID → SOOL + H2O
2LiOH + CO2 → Li2CO3 + H2O
See reaktsioon toimub alati.
5. ALUSELINE OKSIID + HAPPELINE OKSIID → SOOL
CaO + CO2 → CaCO3
See reaktsioon toimub alati ning tekib happelisele oksiidile vastava happe sool.
Ülesanne 5

