Kosmilisest kiirgusest tuumajaamani
Aatom
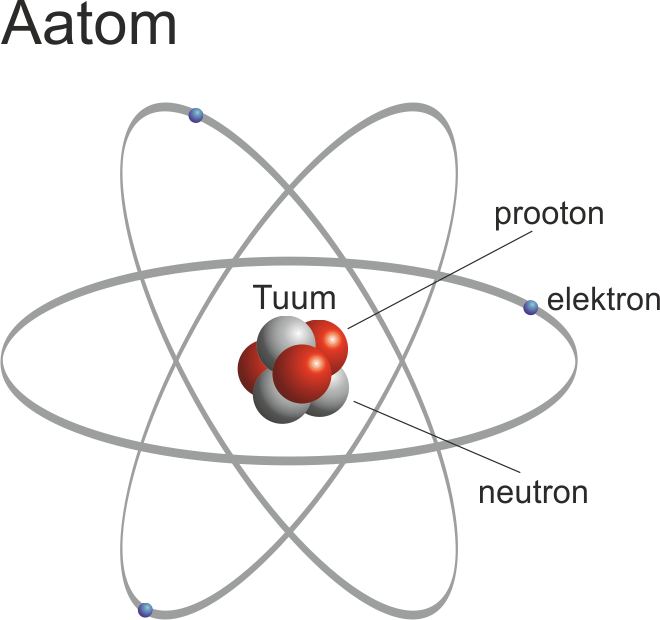 Meid ümbritsevas maailmas koosnevad kõik ained aatomitest. Teadlased Rutherford ja Bohr tegid möödunud sajandi algul kindlaks, et iga aatom omakorda koosneb väikesest positiivse laenguga tuumast, mille ümber keerlevad negatiivse laenguga elektronid.
Meid ümbritsevas maailmas koosnevad kõik ained aatomitest. Teadlased Rutherford ja Bohr tegid möödunud sajandi algul kindlaks, et iga aatom omakorda koosneb väikesest positiivse laenguga tuumast, mille ümber keerlevad negatiivse laenguga elektronid.
Aatomituum sisaldab prootoneid, mis kannavad elektronide negatiivse laenguga võrdset positiivset laengut, ja neutronid, millel laeng puudub. Kuna aatomi tuumas sisalduvate prootonite arv on sama suur kui tuuma ümber tiirlevate elektronide arv, siis on aatom elektriliselt neutraalne. Kuna prootonid ja neutronid on palju raskemad kui elektronid, siis koondub enamus aatomi massist selle tuuma. Elektronide arv aatomis – ja vastavalt prootonite arv tuumas, mida nimetatakse aatomnumbriks – annab elemendile tema unikaalsed omadused. Prootonite ja neutronite koguarvu nimetatakse massiarvuks. Kuna prootonite arv on igale elemendile ainuomane, siis kasutatakse sageli elemendi nimetust koos massiarvuga.
Sama elemendi nukliide, millel on ühesugune prootonite arv, kuid erinev neutronite arv, kutsutakse selle elemendi isotoopideks. Näiteks vesinikul on kolm isotoopi: vesinik-1 (tavaline vesinik, mille tuumas on ainult üks prooton), vesinik-2, mida kutsutakse deuteeriumiks (üks prooton ja üks neutron) ja vesinik-3, mida kutsutakse triitiumiks (üks prooton ja kaks neutronit).
Harjutus:
Uraan on keemiline element järjenumbriga 92, mis kuulub aktinoidide rühma. Välimuselt on uraan hõbevalge metall. Kõik uraani isotoobid on radioaktiivsed. Looduslikust uraanist on 99% uraan-238. Vasta järgmistele küsimustele uraan-238 kohta:

1. Mis on selle keemilise elemendi massiarv?
Õige!
|
Pole õige!
|
Pole õige!
|
2. Mitu prootonit on selle keemilise elemendi tuumas?
Pole õige!
|
Õige!
|
Pole õige!
|
3. Mitu neutronit on selle keemilise elemendi tuumas?
Pole õige!
|
Pole õige!
|
Õige!
|
4. Mitu elektroni tiirleb ümber tuuma?
Pole õige!
|
Õige!
|
Pole õige!
|


