4.9. Metallide korrosioon
Korrosioon on metalli hävinemine ümbritseva keskkonna mõjul.
Metalle kasutatakse väga laialdaselt tööstuses ja igapäevaelus. Metallidel on materjalina suured eelised: hea plastilisus, tugevus, elektri- ja soojusjuhtivus. Samas on neil ka suur puudus – paljud metallid ei ole keemiliselt vastupidavad. Metallid reageerivad õhus, vihmavees ja pinnases olevate ainetega, moodustades oksiide, karbonaate, sulfiide jt. Korrosioon on metalli hävinemine ümbritseva keskkonna mõjul. Metalli korrosioon on redoksreaktsioon, kus metall on redutseerija.
Allikas: https://youtu.be/EwiL-4H361U
Leelis- ja leelismuldmetallide ( IA ja IIA rühma metallid) korrosioon on väga kiire. Seda nägid ka eelnevatest peatükkidest, kus metalli pinna lõikamisel kattus metalli läikiv pind kiiresti tuhmi oksiidikihiga. Raua korrosioon on pigem aeglane protsess ja raua pinnale tekib pikema aja jooksul punakaspruun roostekiht (Fe2O3·nH2O). Raua korrosiooni nimetatakse ka roostetamiseks ning selle tulemusena võib hävineda kogu metall. Kuna rauda kasutatakse väga laialdaselt, siis tekitab raua korrosioon olulist majanduslikku kahju.
Vasel ja hõbedal korrodeerub ainult metalli pindkiht. Vask muutub hallikaksroheliseks vask(II)hüdroksiidkarbonaadi ((CuOH)2CO3) tekke tõttu. Hõbeda pinnale tekib hõbeoksiid või hõbesulfiid (Ag2O, Ag2S).
Metallide korrosioon on isevooluline protsess. Metallist moodustub tagasi ühend, millena ta ka looduslikult esineb. Korrosioonil tekkinud ühendid on püsivad. Korrosioonile vastupidine protsess on metalli tootmine maagist, milleks tuleb kulutada väga palju energiat. Joonisel 1 on toodud lihtsustatud energiadiagramm, mis näitab metalli muutumist metalliühendiks.
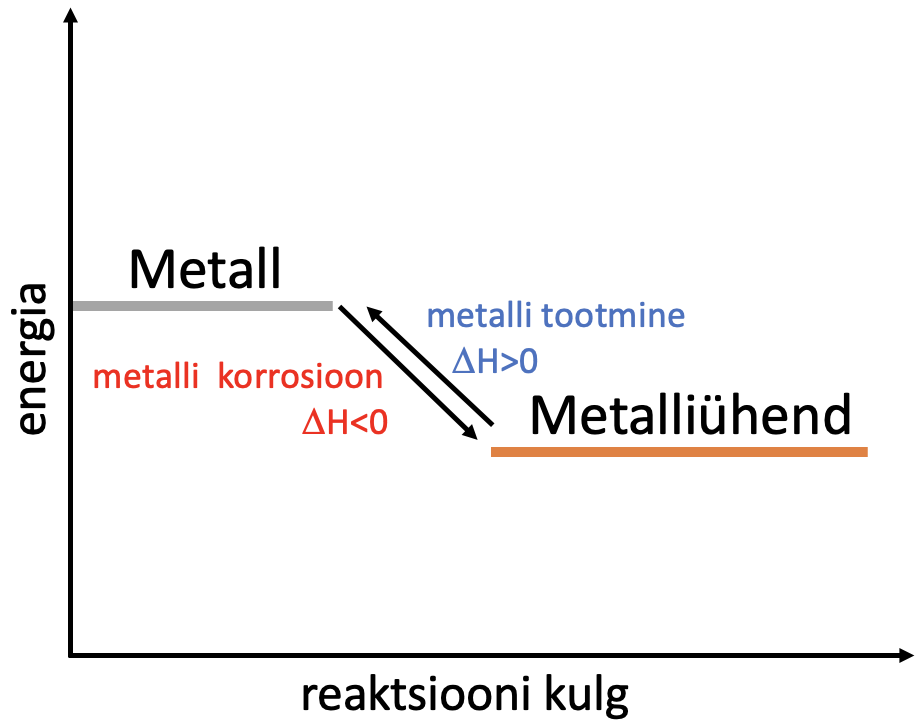
Joonis 1. Metalli ja metalliühendi energiadiagramm
Keemiline korrosioon
Keemiline korrosioon toimub otseses reaktsioonis metalli ja keskkonnas leiduvate oksüdeerijatega, eelkõige kuivade gaaside (hapnik, kloor) või orgaaniliste vedelike (bensiin, õlid) keskkonnas. Tüüpilisemad näited on siin keemiatööstuse reaktorid, automootorid, kuumutusahjud jne.
2 Na (t) + O2(g) → Na2O2(t) keemiline korrosioon
2 Na (t) + O2(g) → 2 Na2O(t) keemiline korrosioon
2 Fe(t) + 3 Cl2(g) $\xrightarrow{temp}$ 2 FeCl3(t) keemiline korrosioon
3 Fe(t) + 2 O2(g) $\xrightarrow{temp}$ Fe3O4(t) kuumutamisel keemiline korrosioon
Elektrokeemiline korrosioon
Elektrokeemiline korrosioon on oluliselt levinum kui keemiline korrosioon. Elektrokeemiline korrosioon leiab aset elektrolüüdilahuses, milleks võib olla ka õhuke veekiht, mis tekib metalli pinnale niiskes õhus ja milles on lahustunud õhus sisalduvad ained.
Tavatingimustes korrodeeruvad veega ainult aktiivsemad metallid. Väheaktiivsete metallide korrodeerumiseks ei ole vesi piisavalt tugev oksüdeerija.
2 Na (t) + 2 H2O(v) → 2 NaOH(l) + H2(g) elektrokeemiline korrosioon
Happelises lahuseks on oksüdeerijaks vesinikioon:
Fe(t) + 2 HCl(l) → FeCl2(l) + H2(g) elektrokeemiline korrosioon
Viimase võrrandi saab kirjutada järgmiste poolreaktsioonidena:
Fe(t) - 2e- → Fe2+(l) toimub raua oksüdeerumine
Vabanenud elektronid kasutatakse ära teises poolreaktsioonis:
2H+(l) + 2e- → H2(g).
Need kaks poolreaktsiooni võivad toimuda metalli erinevates piirkondades. Korrodeerumine saab toimuda seni, kuni jätkub vesinikioone. Kaks poolreaktsiooni kokku võttes saab kirjutada summaarse ioonvõrrandi:
Fe(t) + 2H+(l) → Fe2+(l) + H2(g).
Juhul, kui ei ole tegemist neutraalse lahusega, on enamasti põhiliseks oksüdeerijaks vees lahustunud õhuhapnik (O2), mida on õhus 21 mahuprotsenti. Hapniku redutseerumisel tekib aluseline keskkond:
O2 (g)+ 2H2O(v) +4e- → 4OH-(l)
Hüdroksiidioonide toimel tekivad algul Fe2+-ioonid, mis oksüdeeruvad õhuhapniku toimel edasi Fe3+-ioonideks. Raua pinnale tekib rooste (Fe2O3× nH2O), mis on muutuva koostisega (vaata joonist 2).
4Fe(t) + 3O2(g) + nH2O(v) → 2Fe2O3 nH2O(t)
Igapäevaelus laialdaselt tundud roostetamine ongi raua elektrokeemiline korrosioon neutraalses elektrolüüdilahuses.
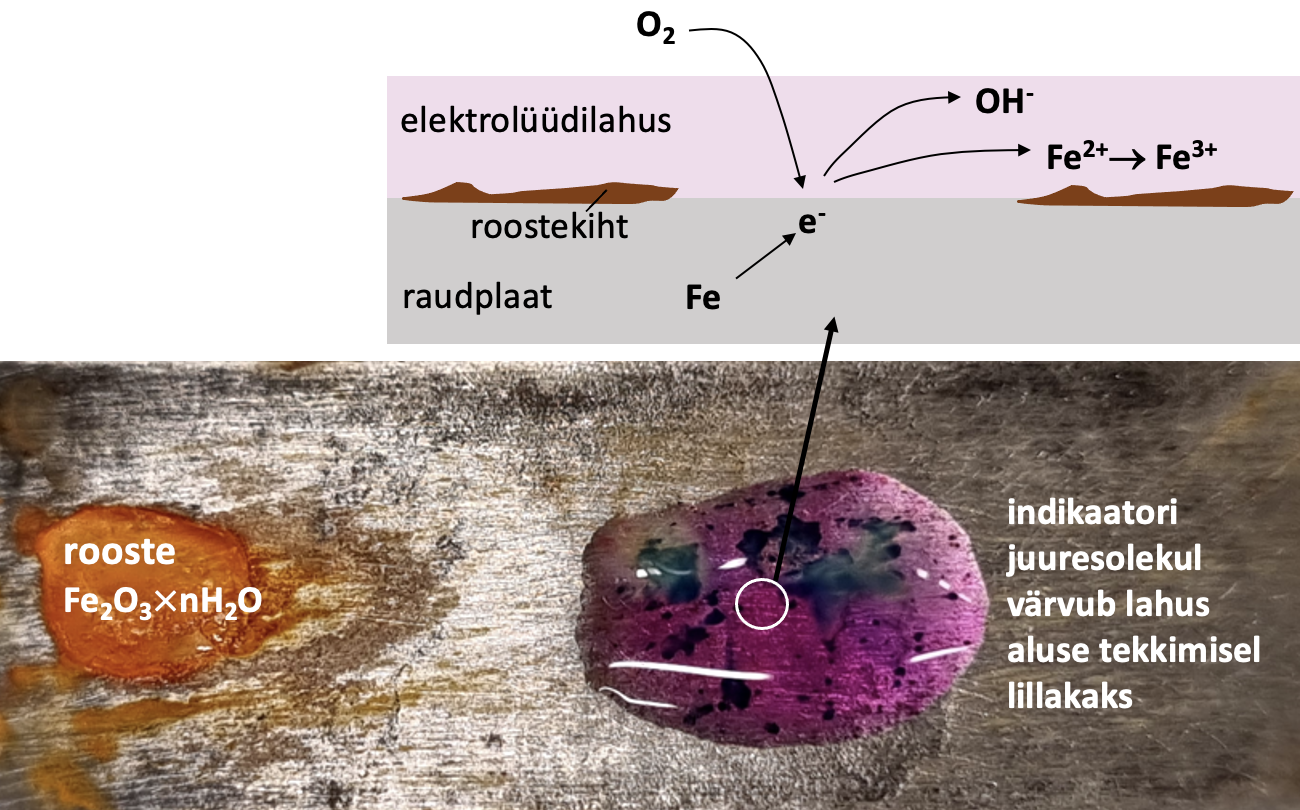
Joonis 2. Raua elektrokeemiline korrosioon neutraalses lahuses
Korrosioonitõrje
Korrosioon tekitab majanduslikult väga palju kahju. Metallidest valmistatud seadmed, konstruktsioonid ja masinad võivad muutuda kasutuskõlbmatuks metallide hävimise tõttu. Selle vältimiseks rakendatakse erinevaid korrosioonitõrje meetodeid.
- Metall isoleeritakse väliskeskkonnast lakkimise, värvimise või emailimise teel. Leiab kasutust eelkõige masinate, seadmete ja suurte metallkonstruktsioonide korral. Isoleerimiseks kasutatakse sageli ka metalli katmist mõne polümeerse kilega (plastikuga).
- Metalli katmine teise, vähem aktiivse metalli kihiga. Pinnale kantav metall on vähem aktiivne ja seetõttu korrosioonikindlam. Eriti dekoratiivne on esemete kulla või hõbedaga katmine. Katmine toimub elektrolüüsi teel. Hävineb kõigepealt vähem aktiivne metall. Korrosioonikaitse on tõhus senikaua, kui kattekoht on vigastamata.
- Metalli katmine aktiivsema metalliga. Igapäevaelus kaetakse metallvõrke, vihmaveetorusid ja veeämbreid tsingiga. Eriti vastupidavad ja dekoratiivsed on näiteks kroomitud autodetailid. Aktiivsem metall hakkab korrodeeruma, aga moodustab tugeva oksiidikihi, mis kaitseb alusmetalli. Aktiivsema metalli kiht kaitseb põhimetalli ka siis, kui pindkiht on kahjustatud. Seetõttu on see ka tõhusam korrosioonitõrje meetod kui vähem aktiivse metalliga katmine.
- Elektrokeemiline kaitse leiab kasutust laevakerede või maa-aluste metalltorude kaitsmisel. Kaitstav ese ühendatakse juhtme abil aktiivsemast metallist plaadiga, mis oksüdeerub. Loovutatud elektronid liiguvad juhtme kaudu kaitsvale metallesemele, kus toimub redutseerumine vesinikioonide ja hapniku molekulide osavõtul.
- Kasutatakse ka korrosiooni aeglustajaid, mida nimetatakse inhibiitoriteks. Need võivad olla väga erinevad anorgaanilised või orgaanilised ained. Näiteks titaani ja alumiiniumi pinnale tekitatakse oksiidikiht (TiO2, Al2O3), mis kaitseb metalli hävinemise eest.