7.3. Amiinid
Allikas: https://youtu.be/PrAQtF6xAbY
Amiinid saadakse ammoniaagi molekulis ühe või mitme vesinikuaatomi asendamisel alküülrühmaga. Vastavalt sellele, kas asendatud on üks, kaks või kolm vesinikku, jaotatakse amiine primaarseteks, sekundaarseteks ja tertsiaarseteks amiinideks. Amiinid on tihti ebameeldiva lõhnaga (nt kala- või laibalõhn) ained, mida looduses tekib eriti orgaaniliste ainete lagunemisel.
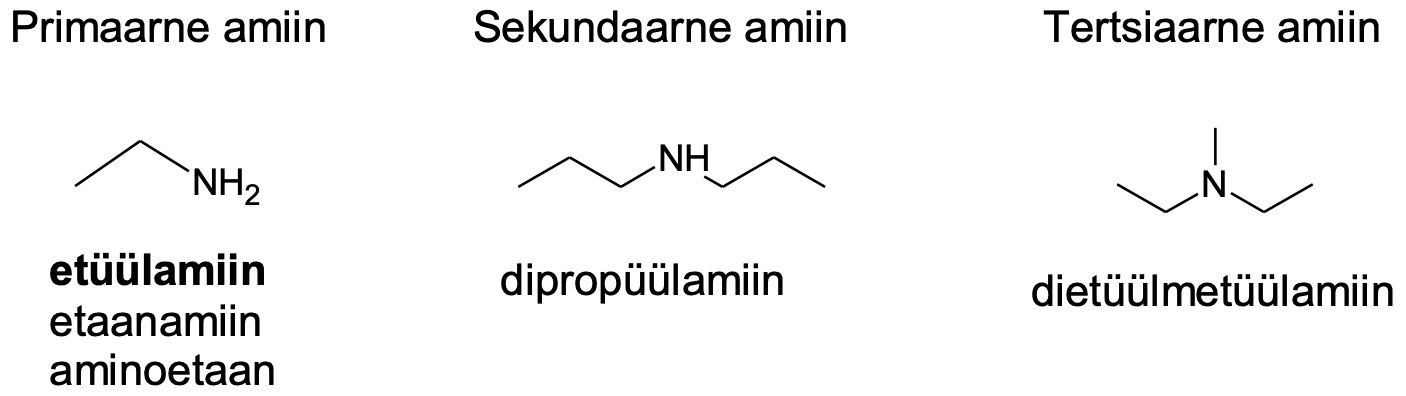
Joonis 1. Näiteid amiinidest
Etüülamiin on esimese aine kõige levinum nimetus, aga korrektsed on ka etaanamiin ja aminoetaan. Eesliide „amino“ on –NH2 korral eelistatud keerukamate ühendite nimetamisel.
Amiinide omadused
Amiinid on polaarsed ja hüdrofiilsed ained.
Amiinid on polaarsed ja hüdrofiilsed ained. Sarnaselt alkoholidele annavad primaarsete ja sekundaarsete amiinide molekulid omavahel vesiniksidemeid. Kuna amiinimolekulide vahel on nõrgemad vesiniksidemed kui alkoholimolekulide vahel, on amiinide keemistemperatuurid üldiselt madalamad kui võrreldava suurusega alkoholidel, kuid siiski kõrgemad kui mitte- või vähepolaarsetel ühenditel.
Tabel 1. Lihtsamate amiinide keemistemperatuurid
|
Amiin |
CH3NH2 |
CH3CH2NH2 |
CH3(CH2)2NH2 |
CH3(CH2)3NH2 |
CH3(CH2)4NH2 |
|
Keemis-temperatuur, °C |
–6 |
18 |
49 |
78 |
102 |
Amiinid on sarnaselt ammoniaagiga nõrgad alused ning reageerivad hapetega, andes vastava ammooniumsoola. Nagu ammoniaagi puhul, toimub ka aminorühma reaktsioon happega nii, et lämmastiku vaba elektronipaar seob vesinikiooni.

Joonis 2. Propüülamiini reaktsioon vesinikkloriidhappega

